Jeûne, graisses et physique : combiner la thérapie cétogène et la radiothérapie contre le cancer
Par CrossFit
Cette revue de 2017 résume les avantages potentiels d'un régime cétogène parallèlement à la radiothérapie.
La radiothérapie est limitée par les dommages qu'elle cause aux cellules saines. Par conséquent, tout traitement simultané qui peut augmenter les dommages causés par la radiothérapie aux cellules cancéreuses ou protéger les cellules saines des dommages peut augmenter son efficacité. On pense que la radiothérapie fonctionne en grande partie en causant des dommages oxydatifs à l'ADN dans le noyau et/ou les mitochondries ; avec des dommages suffisants, la cellule n'est plus capable de se répliquer ou de survivre.
L'idée que le cancer est une maladie métabolique - et, par extension, que les thérapies métaboliques peuvent affecter la progression du cancer - a pris de l'importance avec les travaux d'Otto Warburg dans les années 1920, qui ont découvert que les cellules tumorales excrètent de grandes quantités de lactate même lorsque l'oxygène est disponible. Cette observation suggère qu'il existe des différences métaboliques significatives entre les cellules cancéreuses et les cellules saines. Tout au long des années 1920 et dans les années 1950, d'autres se sont appuyés sur les travaux de Warburg, dont Wilhelm Brünings, qui a fourni des preuves préliminaires que la suppression de la glycémie pouvait réduire la croissance tumorale.
On pense que cette adaptation métabolique offre de multiples avantages aux cellules cancéreuses. Comme Warburg l'a supposé plus tard et d'autres (dont Thomas Seyfried) l'ont observé, les cellules cancéreuses présentent fréquemment des mitochondries défectueuses. Ces cellules sont soit limitées dans leur capacité à achever la respiration aérobie (c'est-à-dire la forme de métabolisme du glucose favorisée par les cellules saines lorsque l'oxygène est disponible), soit ne peuvent le faire qu'en produisant de grandes quantités d'espèces réactives de l'oxygène. Ceci est particulièrement important, car la glycolyse aérobie - la forme de métabolisme favorisée par les cellules cancéreuses - permet aux cellules cancéreuses de répondre à leurs besoins énergétiques en utilisant un processus métabolique alternatif qui limite la production d'espèces réactives de l'oxygène tout en produisant simultanément les « éléments constitutifs » cellulaires (c. squelettes carbonés et azotés) nécessaires à la croissance et à la réplication rapides des cellules. Cette voie produit également de grandes quantités de molécules anti-oxydantes qui contrecarrent les dommages oxydatifs induits par la radiothérapie. Cette voie métabolique alternative, cependant, nécessite que les cellules tumorales consomment beaucoup plus de glucose que les cellules saines ; la glycolyse aérobie produit moins d'énergie par molécule de glucose consommée que la respiration aérobie, donc plus de glucose est nécessaire pour générer la même quantité d'énergie.
Depuis les années 1990, au moins 24 rapports ont été publiés dans lesquels un total de 200 patients ont été traités à l'aide d'un régime cétogène. Les auteurs affirment que le régime cétogène a des effets bénéfiques sur chacun des cinq facteurs, communément appelés les « 5 R de la radiobiologie », résumés ci-dessous, et ils soutiennent donc que le régime améliore l'impact de la radiothérapie sur les cellules cancéreuses tout en atténuant les dommages de la radiothérapie. aux cellules normales. En bref:
· Un régime cétogène, par le biais de mécanismes liés à la privation d'énergie et à d'autres voies de signalisation, réduit la capacité des cellules cancéreuses à réparer l'ADN. Cela augmente l'efficacité de la radiothérapie en empêchant les cellules cancéreuses qui sont endommagées mais non tuées au cours d'un cycle de radiothérapie de récupérer avant les séances suivantes.
· Un régime cétogène ralentit la croissance tumorale et le repeuplement, empêchant la repousse tumorale entre les séances de radiothérapie.
· Un régime cétogène fait passer les cellules saines d'un état anabolique/centrée sur la croissance à un état sans division. Ce changement protège les cellules saines contre les méfaits de la radiothérapie.
· Un régime cétogène réduit l'accès des cellules tumorales au glucose, augmentant la production d'espèces réactives de l'oxygène parmi les tumeurs bien oxygénées (en poussant le métabolisme vers la respiration aérobie) tout en privant d'énergie les tumeurs mal oxygénées.
· Un régime cétogène empêche les cellules cancéreuses de réguler positivement la glycolyse (en réduisant l'accès à son substrat le plus important : le glucose), ce qui empêche simultanément les tumeurs de produire des molécules anti-oxydantes et augmente la production de molécules pro-oxydantes ; simultanément, les cellules saines dotées de mitochondries fonctionnelles augmentent leur potentiel antioxydant grâce au métabolisme des cétones. Le résultat est une vulnérabilité accrue des cellules cancéreuses et une vulnérabilité réduite des cellules saines aux dommages oxydatifs induits par les rayonnements.

Les principaux effets d'un régime cétogène, qui réduit les niveaux de glucose et d'insuline et augmente les niveaux de cétone, sur les cellules saines et cancéreuses sont résumés dans la figure 2 ci-dessous.
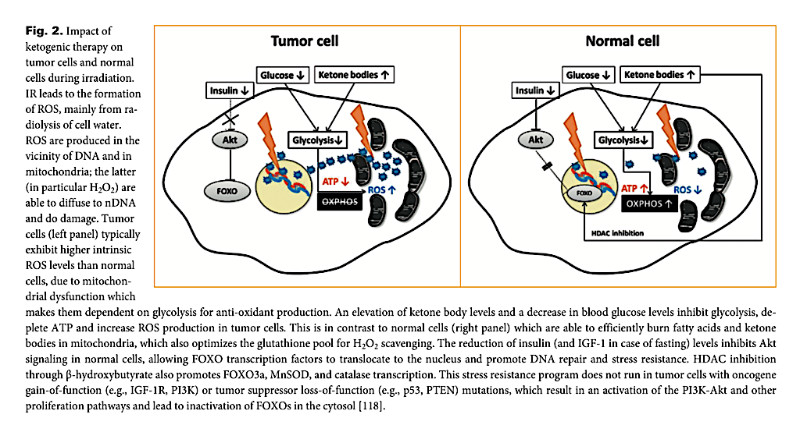
Ces effets et d'autres d'un régime cétogène sur un métabolisme normal et sain devraient augmenter la vulnérabilité des cellules cancéreuses à la radiothérapie et réduire les dommages causés aux cellules saines environnantes. En pratique, cette théorie est cohérente avec les preuves préliminaires chez le rat (1) et l'homme (2) suggérant que l'ajout d'un régime cétogène à un régime de radiothérapie réduit systématiquement la gravité des effets secondaires induits par la radiothérapie et, dans certains cas, augmente l'impact de la radiothérapie sur les tumeurs.
En résumé, les auteurs de cette revue soutiennent qu'un régime cétogène augmente la vulnérabilité des cellules cancéreuses à la radiothérapie et protège les cellules saines des effets néfastes de la radiothérapie en grande partie en raison de ses effets sur les dommages oxydatifs dans chaque type de cellule. Dans les cellules saines, un régime cétogène augmente la production de molécules antioxydantes tout en déplaçant les cellules vers un état qui réduit les effets néfastes des dommages oxydatifs tout en augmentant la réparation. Dans les cellules cancéreuses, le régime alimentaire augmente la production de molécules pro-oxydantes et diminue la production de molécules anti-oxydantes tout en déplaçant les cellules cancéreuses vers un état de privation d'énergie. Les recherches futures testeront si ces avantages théoriques conduisent à une efficacité améliorée de la radiothérapie chez l'homme.
Retrouvez l'article original ici.